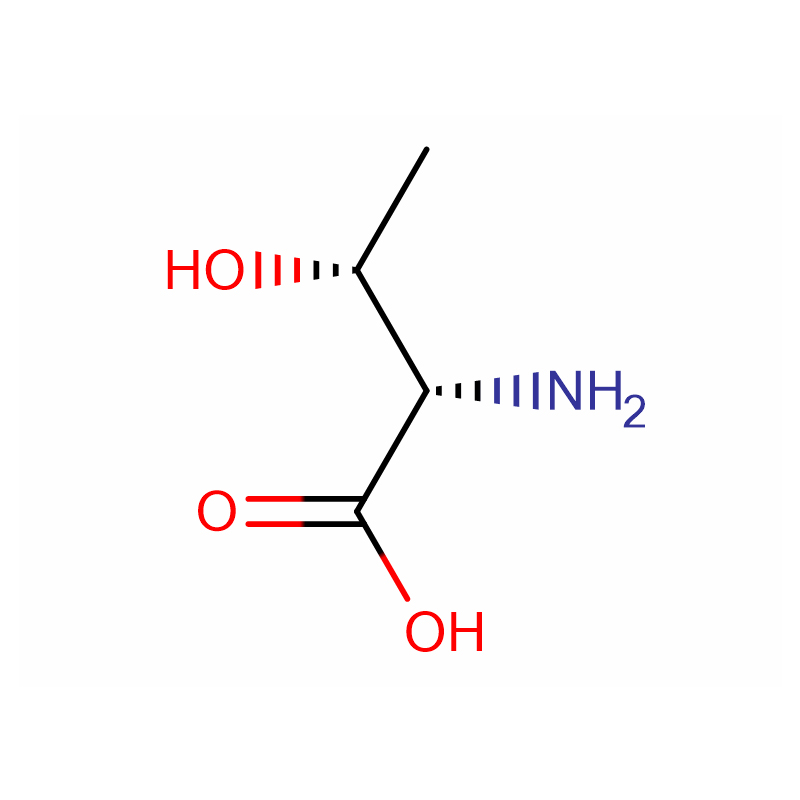
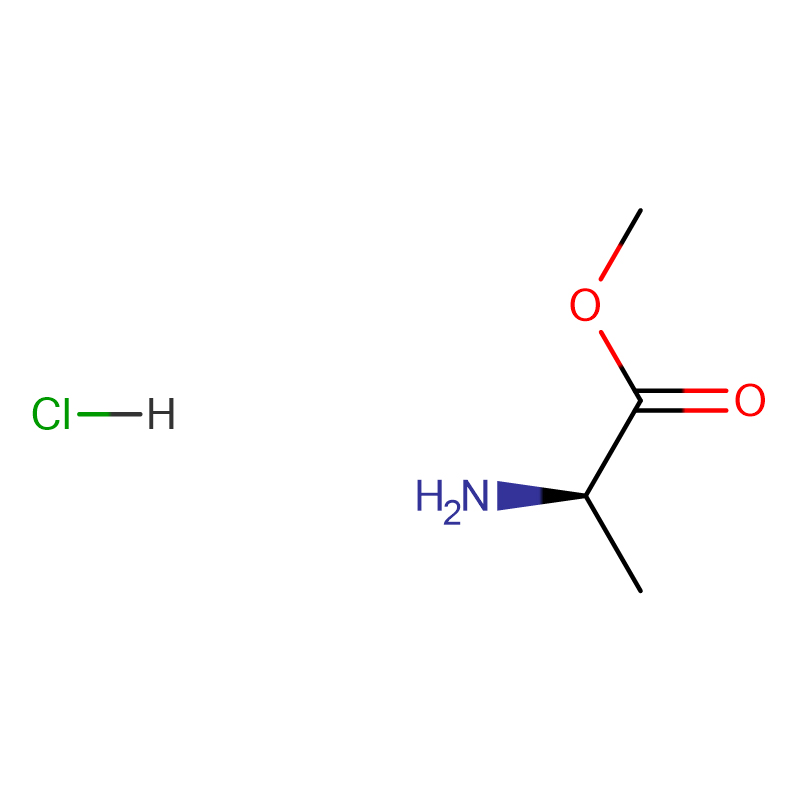
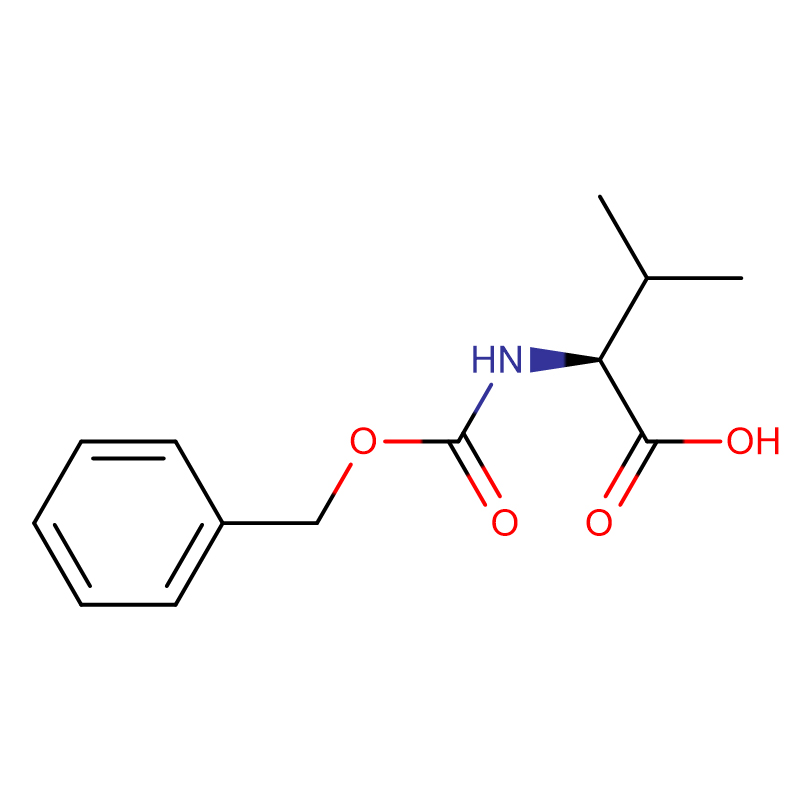
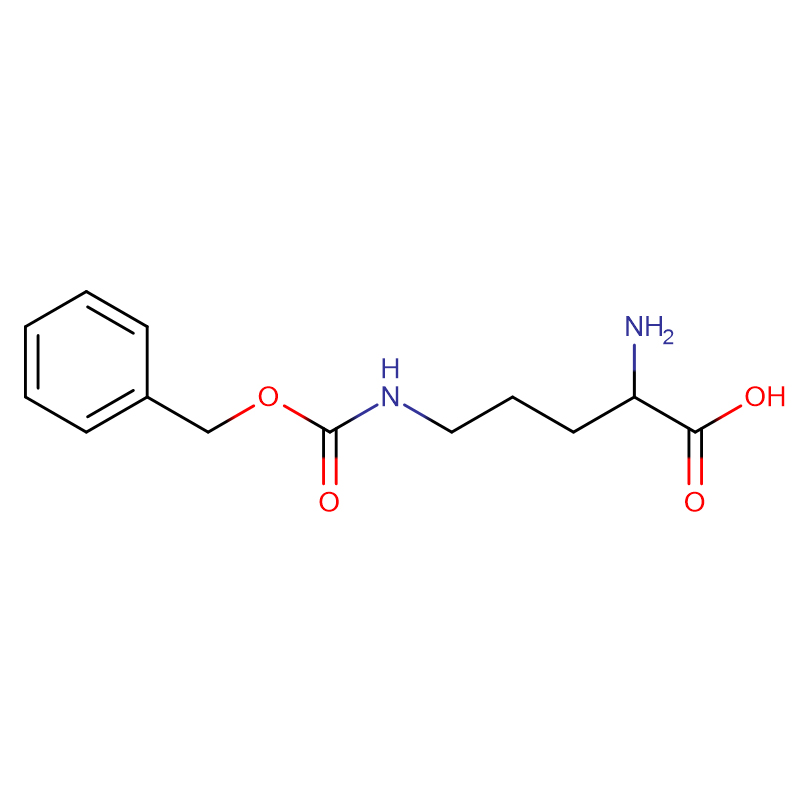
Kyselina (2S,3R)-2-amino-3-hydroxybutanová Cas: 72-19-5 99% Bílý krystalický prášek
| Katalogové číslo | XD90285 |
| jméno výrobku | Kyselina (2S,3R)-2-amino-3-hydroxybutanová |
| CAS | 72-19-5 |
| Molekulární vzorec | C4H9NO3 |
| Molekulární váha | 119,11916 |
| Podrobnosti o úložišti | Okolní |
| Harmonizovaný celní kód | 29225000 |
Specifikace produktu
| Zkouška | 99–101 % |
| Vzhled | Bílý krystalický prášek |
| Specifická rotace | -27,5 až -29,0 |
| Těžké kovy | 10 str./min Max. |
| AS | Max. 10 str./min |
| pH | 5,2 - 6,5 |
| SO4 | <0,020 % |
| Fe | Max. 10 str./min |
| Ztráta sušením | <0,20 % |
| Zbytek po zapálení | <0,10 % |
| Propustnost | NLT 98 % |
| Cl | <0,02 % |
| Amonná sůl | <0,02 % |
Serinové/threoninové proteinové fosfatázy byly popsány u mnoha patogenních bakterií jako esenciální enzymy účastnící se na fosforylaci závislých signálních transdukčních drah a často spojované s virulencí těchto organismů.Inspekce genomu Mycoplasma synoviae odhalila přítomnost genu (prpC) kódujícího domnělou protein fosfatázu podrodiny protein fosfatázy 2C (PP2C).Zde uvádíme úplnou biochemickou charakterizaci fosfatázy M. synoviae (PrpC) a konkrétní roli kovových iontů ve vztahu mezi strukturou a funkcí tohoto enzymu.Analýza aminokyselinové sekvence PrpC odhalila, že všechny zbytky zahrnuté v centru dvoujaderného kovu a domnělé zbytky koordinující iont třetího kovu, konzervované ve fosfatázách PP2C, jsou přítomny v PrpC.PrpC je monomerní protein schopný defosforylovat fosfo-substráty v závislosti na Mn(2+) iontech.Analýza tepelné stability prokázala stabilitu enzymu při mírných teplotách a vliv Mn(2+) iontů na tuto vlastnost.Analýza hmotnostní spektrometrií naznačila, že se na PrpC vážou tři kovové ionty, z nichž dva se zjevně vysokou afinitní konstantou.Mutační analýza předpokládaných třetích zbytků koordinujících kov, Asp122 a Arg164, odhalila, že tyto varianty vykazovaly slabší vazbu manganových iontů a že obě mutace ovlivnily aktivitu PrpC fosfatázy.Podle těchto výsledků je PrpC člen proteinové fosfatázy závislý na kovu se zlepšenou stabilitou v holo formě a s Asp122, pravděpodobně zapojeným do třetího místa vázajícího kov, nezbytným pro katalytickou aktivitu.