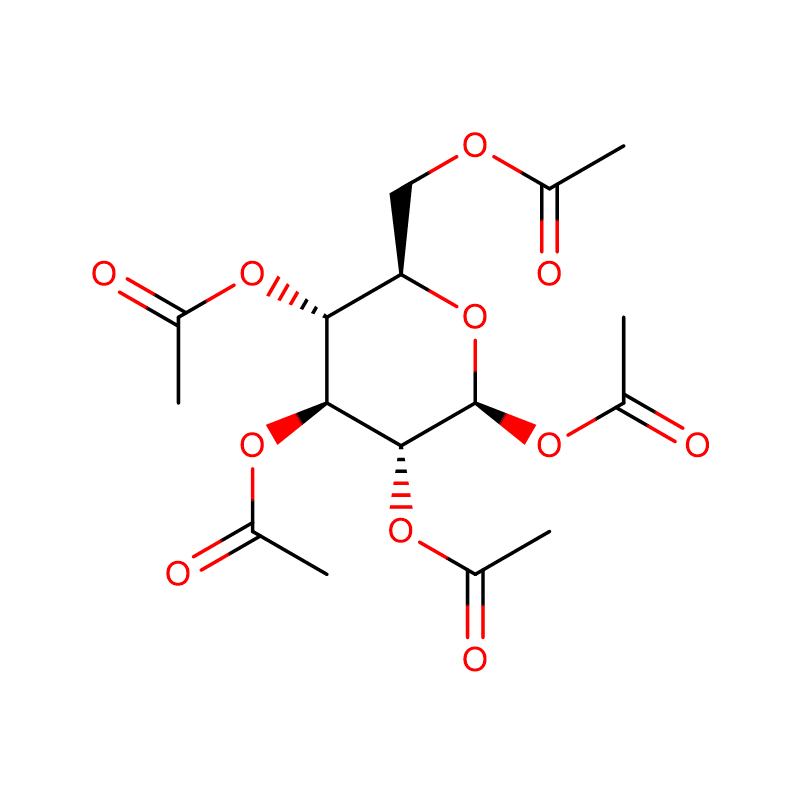
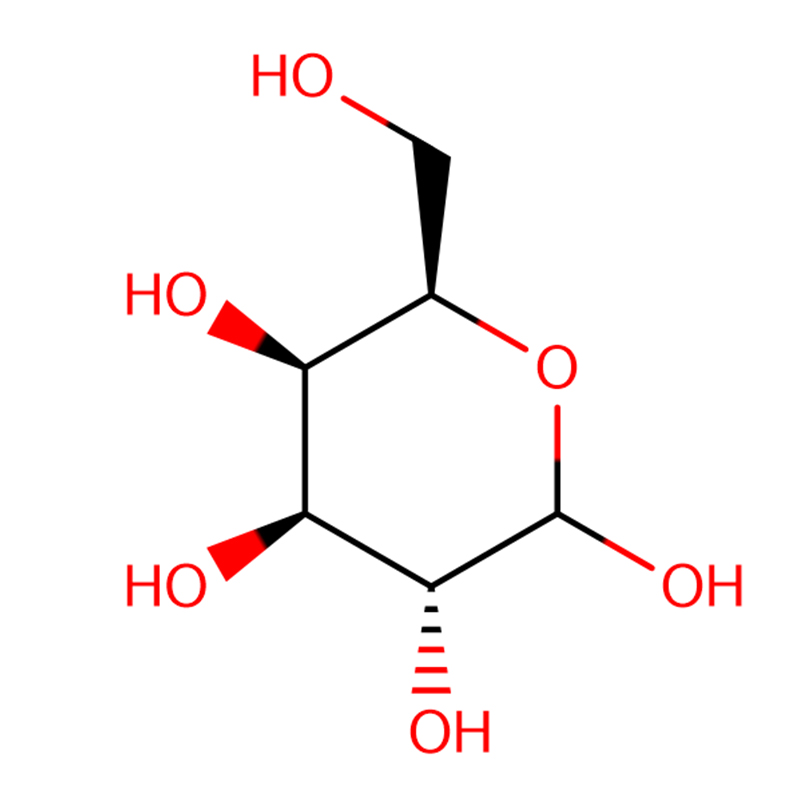
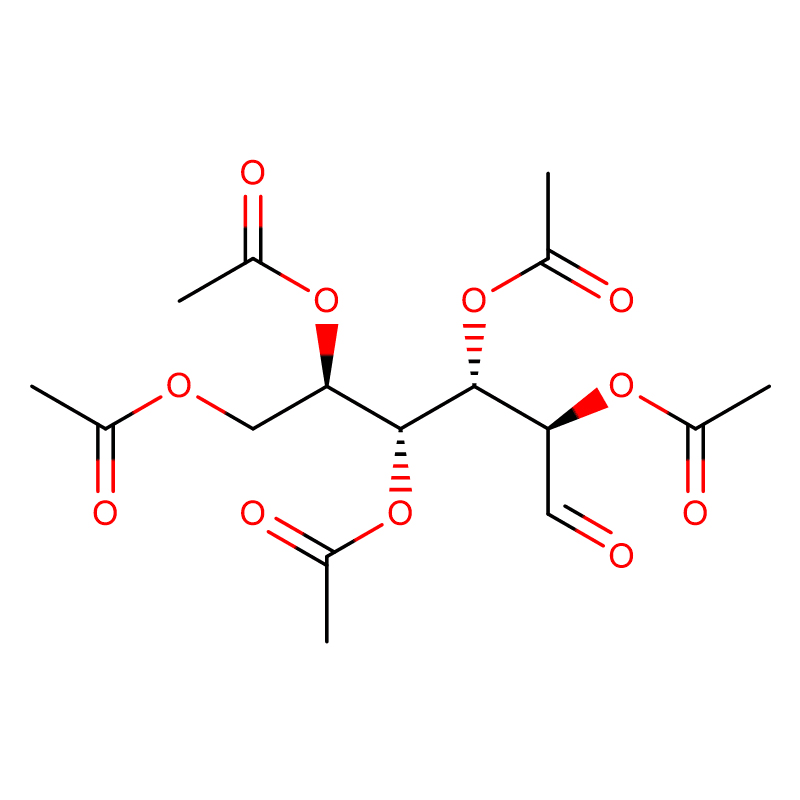
4-NITROFENYL-ALPHA-D-MANNOPYRANOSID CAS:10357-27-4 Off-White Powder 98%
| Katalogové číslo | XD90011 |
| jméno výrobku | 4-Nitrofenyl-alfa-D-mannopyranosid |
| CAS | 10357-27-4 |
| Molekulární vzorec | C12H15NO8 |
| Molekulární váha | 30301.25 |
| Podrobnosti o úložišti | -2do -8°C |
| Harmonizovaný celní kód | 29400000 |
Specifikace produktu
| Voda | <5 % Karl Fische |
| Rozpustnost | 1 % v DMF je čirý a bezbarvý |
| Čistota | Volný 4-nitrofenol <200 ppm |
| HPLC | >98 % |
| Vzhled | Špinavě bílý prášek |
Mechanistický pohled na Ca2+-dependentní rodinu alfa-manosidáz u lidského střevního symbionta.
Bakterie tlustého střeva, jejichž příkladem je Bacteroides thetaiotaomicron, hrají klíčovou roli při udržování lidského zdraví tím, že využívají velké rodiny glykosidhydroláz (GH) k využití dietních polysacharidů a hostitelských glykanů jako živin.Příkladem takové expanze rodiny GH je 23 glykosidáz rodiny GH92 kódovaných genomem B. thetaiotaomicron.Zde ukazujeme, že se jedná o alfa-manosidázy, které působí prostřednictvím jediného vytěsňovacího mechanismu pro využití hostitelských N-glykanů.Trojrozměrná struktura dvou manosidáz GH92 definuje rodinu dvoudoménových proteinů, ve kterých je katalytické centrum umístěno na rozhraní domény a poskytuje kyselou (glutamát) a zásadu (aspartát) podporu hydrolýze v Ca(2+)- závislým způsobem.Trojrozměrné struktury GH92 v komplexu s inhibitory poskytují pohled na specifičnost, mechanismus a konformační itinerář katalýzy.Ca(2+) hraje klíčovou katalytickou roli tím, že pomáhá deformovat mannosid od jeho základního stavu (4)C(1) židle směrem k přechodnému stavu.(Bibliografie: Nat.Chem.Biol.6, 125-32, (2010)
Frontální afinitní chromatografie ovalbuminových glykoasparaginů na koloně concanavalin A-sepharose.Kvantitativní studie vazebné specificity lektinu.
Interakce konkanavalinu A (ConA) imobilizovaného na Sepharose 4B s 10 glykoasparaginy odvozenými z ovalbuminu byly kvantitativně zkoumány frontální afinitní chromatografií.Při této metodě se na kolonu ConA-Sepharose kontinuálně aplikuje roztok sacharidů a jako parametr síly interakce se měří retardace čela eluce.Lze určit disociační konstantu (Kd) pro každý sacharid s ConA.Analýza vazby p-nitrofenyl-alfa,D-manosidu ukázala, že vazebné vlastnosti ConA se po imobilizaci na Sepharose 4B v podstatě nemění.Každý z ovalbuminových glykoasparaginů byl pro analýzu značen tritiem metodou redukční methylace.Srovnání získaných hodnot Kd ukázalo, že vazba ConA se značně liší s velmi malými strukturálními rozdíly glykosylového řetězce.Výsledky naznačují, že ConA rozpoznává specifickou strukturu glykosylového řetězce, Man alfa 1-6(Man alfa 1-3)Man, ve které by alespoň jedna hydroxylová skupina v poloze C-3 C-6-vázané manózy měla být volná.